榮昌生物:一家本土創(chuàng)新藥企的十三年
來(lái)源:人民日?qǐng)?bào)健康客戶端
2022-04-28 12:26:04
從默默無(wú)聞到聲名鵲起,榮昌生物花了十三年時(shí)間。榮昌生物聯(lián)合創(chuàng)始人、CEO兼首席科學(xué)官房健民告訴人民日?qǐng)?bào)健康客戶端記者,“榮昌生物成立至今始終在面對(duì)一個(gè)根本的問題:如何能走出一條本土新藥創(chuàng)新之路。”
房健民和榮昌生物十三年間的選擇和堅(jiān)持,也是我國(guó)本土創(chuàng)新藥生態(tài)的一個(gè)注腳。根據(jù)金融數(shù)據(jù)分析機(jī)構(gòu)WIND數(shù)據(jù),兩年共有107家醫(yī)藥生物企業(yè)上市,超過此前五年之和,累計(jì)募集資金1427億元。

左二為榮昌生物聯(lián)合創(chuàng)始人、CEO兼首席科學(xué)官房健民博士。受訪者供圖。
十年磨一劍,瞄準(zhǔn)治療領(lǐng)域的空白
榮昌生物成功上市的背后,是中國(guó)創(chuàng)新藥進(jìn)入收獲期。2021年4月20日,全球首個(gè)雙靶點(diǎn)紅斑狼瘡新藥泰它西普誕生在中國(guó)。
泰它西普的起步,要從2008年開始。在國(guó)外待了近20年的房健民決定回國(guó)創(chuàng)業(yè),彼時(shí)本土創(chuàng)新藥物研發(fā)仍一派冷清,我國(guó)獲批的I類新藥只有5個(gè),但在房健民看來(lái),“冷清中孕育著巨大的機(jī)會(huì)。” 2008年,榮昌生物剛成立,在借用的大學(xué)實(shí)驗(yàn)室里,房健民即帶領(lǐng)榮昌生物開始了第一場(chǎng)“冒險(xiǎn)”,瞄準(zhǔn)的治療領(lǐng)域是幾乎一片空白的系統(tǒng)性紅斑狼瘡" 紅斑狼瘡(SLE)。
房健民告訴人民日?qǐng)?bào)健康客戶端記者,系統(tǒng)性"紅斑狼瘡"紅斑狼瘡的治療用藥是新藥研發(fā)領(lǐng)域的一座險(xiǎn)峰,過去幾十年里,國(guó)際上多款新藥都以失敗告終,在當(dāng)時(shí),系統(tǒng)性紅斑狼瘡病人幾乎無(wú)藥可用。
中國(guó)醫(yī)師協(xié)會(huì)風(fēng)濕免疫科醫(yī)師分會(huì)會(huì)長(zhǎng)、北京協(xié)和醫(yī)院風(fēng)濕免疫科主任曾小峰分享一組調(diào)查數(shù)據(jù)顯示,在3萬(wàn)紅斑狼瘡患者中死亡患者達(dá)1000人之多。
“公司剛開始的時(shí)候困難重重,當(dāng)時(shí)有經(jīng)驗(yàn)的技術(shù)人員很難找到,很多基本的技術(shù)都會(huì)出問題,例如,將藥物基因插入到細(xì)胞染色體是泰它西普開發(fā)的早期工作之一,但一開始我們的技術(shù)人員沒有經(jīng)驗(yàn),發(fā)現(xiàn)轉(zhuǎn)基因后的細(xì)胞很快就死了,細(xì)胞都養(yǎng)不活。” 房健民告訴記者。
“由于細(xì)胞培養(yǎng)反復(fù)失敗,有人對(duì)項(xiàng)目發(fā)生懷疑,信心出現(xiàn)動(dòng)搖,認(rèn)為這個(gè)新藥項(xiàng)目不行,當(dāng)時(shí)我的壓力也很大。后來(lái)招到了一位有一定經(jīng)驗(yàn)的細(xì)胞培養(yǎng)工程師,才慢慢解決了問題,使項(xiàng)目走上了軌道。類似的困難不勝枚舉,我們這支年輕的團(tuán)隊(duì)在摸著石頭過河中慢慢成長(zhǎng)起來(lái)。” 房健民回憶,單是從建實(shí)驗(yàn)室到申報(bào)臨床試驗(yàn)這一段路,他們就走了兩年多。
2015年8月,《關(guān)于改革藥品醫(yī)療器械審評(píng)審批制度的意見》發(fā)布,提出了提高審評(píng)審批質(zhì)量、解決注冊(cè)申請(qǐng)積壓。長(zhǎng)期跟蹤藥政改革的南開大學(xué)法學(xué)院教授宋華琳告訴人民日?qǐng)?bào)健康客戶端記者,“此時(shí),藥審中心緊鑼密鼓地參照國(guó)際經(jīng)驗(yàn)調(diào)整了機(jī)構(gòu)設(shè)置,并面向海內(nèi)外高薪引進(jìn)人才,工作人員數(shù)量呈現(xiàn)數(shù)倍增長(zhǎng),初步解決了審評(píng)人員嚴(yán)重缺乏的問題。”
在這個(gè)階段,泰它西普交上了“好運(yùn)”。2015年,泰它西普順利取得了II期臨床試驗(yàn)批件,“接下來(lái)的幾年之中,我們充分利用國(guó)家藥監(jiān)局推出的改革政策,通過與藥審中心不斷溝通,啟動(dòng)了一系列的II期或III期臨床試驗(yàn)。”房健民告訴記者。

研究人員正在實(shí)驗(yàn)室中開展化合物篩選研究工作。受訪者供圖。
2019年,《藥品管理法》迎來(lái)近20年來(lái)最全面的一次修訂,宋華琳認(rèn)為,“此次修訂將審評(píng)制度改革經(jīng)驗(yàn)以法律形式固定了下來(lái),進(jìn)一步推動(dòng)解決此前審批時(shí)間流程過長(zhǎng),解決生產(chǎn)企業(yè)在研發(fā)創(chuàng)新上的積極性不高的問題。”
2020年,我國(guó)共有14個(gè)國(guó)產(chǎn)I類新藥獲批上市,為此前歷年之最。榮昌生物的命運(yùn)也在這一年迎來(lái)重大轉(zhuǎn)折:泰它西普Ⅱ期b關(guān)鍵臨床試驗(yàn)達(dá)到了主要終點(diǎn),數(shù)據(jù)顯示其高劑量組48周應(yīng)答率達(dá)到79.2%,憑借著這一份best-in-class的答卷,泰它西普于2021年成功獲批上市。
“狼瘡靶向藥物研發(fā)中很多藥物都經(jīng)歷了過山車效應(yīng),終止在臨床Ⅲ期,研發(fā)歷程充滿荊棘”。中華醫(yī)學(xué)會(huì)風(fēng)濕病學(xué)分會(huì)主任委員趙巖告訴記者,而榮昌生物泰它西普作為近60年來(lái)首個(gè)雙靶點(diǎn)紅斑狼瘡新藥,實(shí)現(xiàn)了國(guó)內(nèi)首發(fā)第一,也是雙靶標(biāo)治療SLE國(guó)際第一。
新藥“出海”嶄露頭角,療效和質(zhì)量過硬就有底氣
在2021年獲批上市的創(chuàng)新藥中,除了系統(tǒng)性紅斑狼瘡的泰它西普外,榮昌生物研發(fā)的維迪西妥單抗,作為我國(guó)本土首款抗體偶聯(lián)藥物(ADC)也在其中。
維迪西妥單抗
維迪西妥單抗獲批后不久,榮昌生物就與國(guó)際著名生物技術(shù)公司西雅圖基因達(dá)成了一項(xiàng)高達(dá)26億美元的獨(dú)家許可協(xié)議,刷新了當(dāng)時(shí)中國(guó)制藥企業(yè)單品種海外授權(quán)交易的最高紀(jì)錄。
在此之前,抗體偶聯(lián)藥物(ADC)在我國(guó)仍鮮有人問津,但房健民很早就對(duì)ADC藥物感興趣,他告訴記者,“我們?cè)谑昵熬烷_始布局ADC藥物的研發(fā),ADC藥物的特別之處在于,相對(duì)于普通單抗藥物而言,ADC藥物可以更加精準(zhǔn)有效地殺傷腫瘤細(xì)胞,它就像精準(zhǔn)制導(dǎo)的導(dǎo)彈,可以進(jìn)入到敵人碉堡內(nèi)爆炸,達(dá)到最佳的打擊效果。”
而鑒于當(dāng)時(shí)ADC藥物在國(guó)內(nèi)仍是一片空白,監(jiān)管方面也沒有經(jīng)驗(yàn)可循,維迪西妥單抗的臨床試驗(yàn)審批之路充滿挑戰(zhàn)。從生產(chǎn)工藝到質(zhì)量標(biāo)準(zhǔn),從臨床前數(shù)據(jù)到臨床設(shè)計(jì),都有太多的不確定性。
房健民回憶,2014年底到2015年間,由于維迪西妥單抗是我國(guó)第一個(gè)申報(bào)臨床試驗(yàn)的創(chuàng)新ADC藥物,藥監(jiān)部門為此特地召開了兩次閉門交流會(huì),一次會(huì)議甚至開了一天半。
“我們圍繞這個(gè)ADC藥物進(jìn)行了大量研究工作,提供了大量的數(shù)據(jù)。在申報(bào)過程中,我們也盡了最大的努力配合監(jiān)管部門,這個(gè)藥物的審評(píng)工作對(duì)后續(xù)其他ADC藥物的申報(bào)具有重要意義。”房健民說(shuō),雙方的努力最終取得了成果,2015年底,維迪西妥單抗如期獲得了臨床試驗(yàn)批件。
“至于與西雅圖基因的關(guān)系,我們2018年開始就開始了雙方交流,2019年1月,我和西雅圖基因負(fù)責(zé)人首次見面,當(dāng)時(shí)維迪西妥單抗的臨床試驗(yàn)仍在進(jìn)行時(shí),已經(jīng)取得了初步的臨床數(shù)據(jù),2020年在尿路上皮癌、胃癌、乳腺癌等適應(yīng)癥取得了更多的數(shù)據(jù),雙方有了共識(shí)。因此,本土創(chuàng)新藥只要療效和質(zhì)量過硬,就有底氣。”房健民告訴記者。
根據(jù)獨(dú)家全球許可協(xié)議,榮昌生物將維迪西妥單抗在亞洲區(qū)(除日本、新加坡外)以外的臨床開發(fā)和商業(yè)化權(quán)益,授權(quán)給西雅圖基因公司。同時(shí),榮昌生物還獲得了維迪西妥單抗在西雅圖基因區(qū)域凈銷售額從高個(gè)位數(shù)到百分之十幾的梯度銷售收入。
兩地上市,醫(yī)藥創(chuàng)新遇到了最好的時(shí)候
3月31日,榮昌生物宣布在科創(chuàng)板二度IPO上市,募集資金約26億元,已是很多港股和科創(chuàng)上市公司的總市值。上一次這樣的時(shí)刻發(fā)生在2020年11月9日,當(dāng)天,榮昌生物在港交所上市,并以5.9億美元一舉創(chuàng)下當(dāng)年全球生物技術(shù)IPO募資最高紀(jì)錄。
從港交所上市,到登陸科創(chuàng)板,兩地上市的榮昌生物,被業(yè)界稱為中國(guó)生物藥界“新貴”。房健民感慨,榮昌生物趕上了好時(shí)候。
國(guó)家發(fā)改委宏觀經(jīng)濟(jì)研究院生物產(chǎn)業(yè)發(fā)展戰(zhàn)略專家韓祺告訴記者,2018年以前,創(chuàng)新藥企業(yè)一直面臨著一個(gè)共同的痛點(diǎn):融資難。2018年是一個(gè)分水嶺,我國(guó)生物制藥企業(yè)上市熱就是從這一年開啟的。
2018年4月,港交所推出了25年來(lái)最重大的一次上市改革,公開融資的大門首次向未盈利的生物醫(yī)藥公司敞開,首次掀起了醫(yī)藥生物IPO上市熱的潮流。
隨后,大陸科創(chuàng)板、北交所陸續(xù)試點(diǎn)注冊(cè)制,允許未盈利企業(yè)上市,注冊(cè)制的改革對(duì)我國(guó)生物制藥行業(yè)發(fā)展影響深遠(yuǎn),再加上國(guó)家產(chǎn)業(yè)政策的大力扶持,投資者對(duì)熱門賽道的追捧等因素,生物制藥企業(yè)再掀上市熱潮。
中山大學(xué)醫(yī)藥經(jīng)濟(jì)研究所所長(zhǎng)宣建偉告訴記者,科創(chuàng)板、創(chuàng)業(yè)板、北交所多樣化的上市標(biāo)準(zhǔn),大大增強(qiáng)了初創(chuàng)及未盈利醫(yī)藥企業(yè)的上市預(yù)期,中國(guó)醫(yī)藥市場(chǎng)已經(jīng)成為全球范圍內(nèi)炙手可熱的創(chuàng)新市場(chǎng)。
“我國(guó)本土創(chuàng)新已經(jīng)走過了初期‘野蠻生長(zhǎng)’的階段,正在迎來(lái)‘大浪淘沙’的發(fā)展階段,值得期待的是,‘破發(fā)’之后,真正的創(chuàng)新藥一定會(huì)被留下。”宣建偉表示。
本次榮昌生物的融資,將用于推進(jìn)公司核心產(chǎn)品的國(guó)際化開發(fā)以及管線中其他產(chǎn)品的臨床試驗(yàn)推進(jìn)。根據(jù)榮昌生物的招股書,目前,泰它西普治療系統(tǒng)性紅斑狼瘡的美國(guó)III期臨床試驗(yàn)已啟動(dòng),治療IgA腎病的美國(guó)II期臨床試驗(yàn)于2021年9月啟動(dòng)。
目前,榮昌生物的維迪西妥單抗正在開展針對(duì)HER2陽(yáng)性肝轉(zhuǎn)移晚期乳腺癌的III期試驗(yàn)、HER2低表達(dá)乳腺癌III期試驗(yàn)等多個(gè)III期臨床研究;RC28(VEGF/FGF雙融合蛋白)正在推進(jìn)治療濕性年齡相關(guān)黃斑變性、糖尿病黃斑水腫、糖尿病視網(wǎng)膜病變的II期臨床;另有4個(gè)新藥正在開展I期臨床研究。
2022年3月29日,榮昌生物公布2021年財(cái)報(bào),公司全年收入14.24億元,實(shí)現(xiàn)凈利潤(rùn)2.76億元。這也是榮昌生物成立至今,首次實(shí)現(xiàn)盈利。值得關(guān)注的是,榮昌生物的研發(fā)費(fèi)用正大幅增長(zhǎng),2021年全年研發(fā)投入7.11億元。
房健民堅(jiān)持認(rèn)為,榮昌生物的身上帶著強(qiáng)烈的中國(guó)式本土創(chuàng)新的烙印。“雖然起步于缺少創(chuàng)新的土壤,但最后能走到這里,除了我們比別人多了一些最樸實(shí)的堅(jiān)持,每一個(gè)改革的紅利我們都收到了。如今我國(guó)已成一片創(chuàng)新的熱土,我們的創(chuàng)新使命也會(huì)不斷地延續(xù)下去。”(記者 徐婷婷 譚琪欣)
想爆料?請(qǐng)登錄《陽(yáng)光連線》( https://minsheng.iqilu.com/)、撥打新聞熱線0531-66661234或96678,或登錄齊魯網(wǎng)官方微博(@齊魯網(wǎng))提供新聞線索。齊魯網(wǎng)廣告熱線0531-81695052,誠(chéng)邀合作伙伴。

國(guó)網(wǎng)山東電力“一地一案”做實(shí)做細(xì) 秋收保電工作
- [詳細(xì)]
- 國(guó)網(wǎng)山東電力 2024-10-09

東山曉魯|山東出臺(tái)重要舉措!破解縣域經(jīng)濟(jì)發(fā)展不平衡“堵點(diǎn)”
- [詳細(xì)]
- 閃電新聞 2024-10-09

東山曉魯|從“可觀”到“可游”、從“看景”到“入景”:國(guó)慶大數(shù)據(jù)看山東文旅新活力
- [詳細(xì)]
- 閃電新聞 2024-10-08

《潮起東方》首演發(fā)布會(huì)在京舉行,看中國(guó)企業(yè)如何走向世界潮頭
- [詳細(xì)]
- 閃電新聞 2024-10-08

探討文化傳承與發(fā)展 5000位國(guó)學(xué)愛好者共聚雁棲湖
- [詳細(xì)]
- 閃電新聞 2024-10-06

飛馳的山東——天天向上
- [詳細(xì)]
- 閃電新聞 2024-10-06

孫建博:荒山變青山,青山變金山
- [詳細(xì)]
- 原山林場(chǎng) 2024-10-05
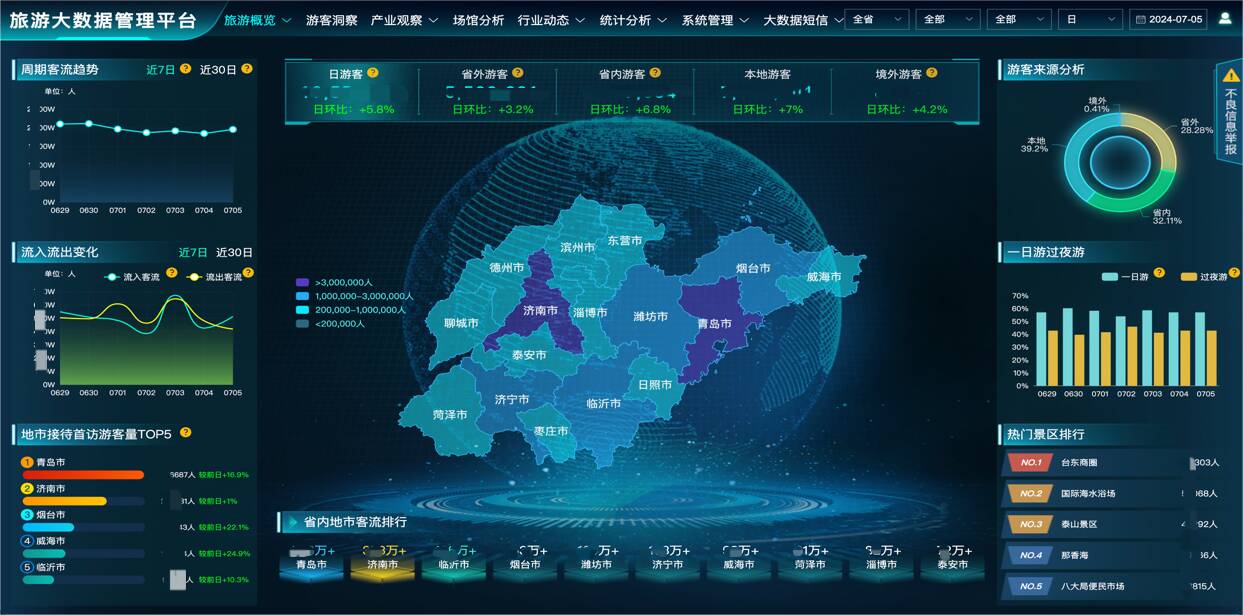
山東移動(dòng)大數(shù)據(jù)賦能齊魯“黃金周”智慧游
- [詳細(xì)]
- 閃電新聞 2024-10-03

迎國(guó)慶 山東多地學(xué)校組織豐富多彩活動(dòng)激發(fā)學(xué)生愛國(guó)情懷
- [詳細(xì)]
- 閃電新聞 2024-10-01

津?yàn)H高鐵站前六標(biāo):1000余名工人堅(jiān)守崗位 奮戰(zhàn)一線
- [詳細(xì)]
- 閃電新聞 2024-10-01

最新進(jìn)展!濟(jì)廣高速改擴(kuò)建工程鄆巨河特大橋合龍
- [詳細(xì)]
- 閃電新聞 2024-10-01
- 領(lǐng)養(yǎng)代替購(gòu)買、文明促進(jìn)和諧泉城寵愛為愛領(lǐng)養(yǎng)活動(dòng)在印象城成功舉辦
- “齊魯號(hào)”團(tuán)隊(duì)用堅(jiān)守護(hù)航山東中歐班列
- 奮進(jìn)之路丨孔子-亞里士多德論壇首次來(lái)中國(guó) 世界儒學(xué)在文明對(duì)話中形成
- 網(wǎng)絡(luò)問政·辦實(shí)事 | 海陽(yáng)市:加強(qiáng)垃圾清運(yùn)管理 及時(shí)清理外溢污水
- 國(guó)慶假期大數(shù)據(jù)|濟(jì)南機(jī)場(chǎng)累計(jì)運(yùn)送旅客45.6萬(wàn)人次
- 1山東棗莊:鄉(xiāng)村興 石榴紅 電先行
- 2山東7個(gè)集體和7名個(gè)人榮獲全國(guó)民族團(tuán)結(jié)進(jìn)步模范集體、模范個(gè)人
- 32024 PT展| 風(fēng)液融合x預(yù)制化,浪潮通信信息推動(dòng)高效綠色數(shù)據(jù)中心建設(shè)
- 4【全國(guó)科普日】特教學(xué)校師生走進(jìn)山東省地質(zhì)災(zāi)害防治科普基地和原山森林生態(tài)科普館
- 5東山曉魯|這一國(guó)際活動(dòng)緣何“花落”青島?
- 6山東省消費(fèi)者協(xié)會(huì)發(fā)布國(guó)慶假期消費(fèi)提示
- 7中秋行囊:無(wú)人機(jī)、大閘蟹、海參……奔赴的是滿滿的愛意

















